جهش ژنتیکی مهمی که عامل بیماری کرون است، سرانجام کشف شد


جهشهای یک ژن مرتبط با بیماری کرون باعث میشوند سلولهای کلیدی ایمنی توانایی تغییر حالت خود را از دست بدهند؛ امری که منجر به واکنش بیشفعال آنها و بروز التهاب میشود.
تغییرات ژن NOD2 پیشتر با بیماری کرون مرتبط شناخته شدهاند، اما نقش دقیق این تغییرات در پاتولوژی بیماری مدتها بهعنوان یک راز باقی مانده بود.
پژوهشگران دانشگاه کالیفرنیا، سندیهگو (UC San Diego) از تکنیکهای یادگیری ماشین برای شناسایی الگوهای فعالیت ژنی سلولهای ایمنی در روده بهره گرفتند.
آزمایشهایی که بر روی سلولهای پرورده در آزمایشگاه و نمونههای گرفتهشده از رودههای سالم و دستگاه گوارش بیماران مبتلا به نوعی کرون بهنام بیماری التهابی روده (IBD) انجام شد، نشان داد که این جهشها با مکانیزمهای حفاظتی معمول که پروتئینهای NOD2 برای مقابله با IBD به کار میبرند، تداخل میکنند.
مرتبط: این مولکولهای آسیبرسان به DNA ممکن است ارتباط بین سرطان روده بزرگ و IBD را توضیح دهند
با پیگیری رفتار سلولهای ایمنی به نام ماکروفاژها از طریق بیان ژنهایشان، پژوهشگران توانستند سلولهایی را شناسایی کنند که به حفظ سلامت روده کمک میکنند و سلولهایی که به حالت التهابی در میآیند و باعث آسیب میشوند.
“روده یک میدان نبرد است و ماکروفاژها نگهبانان صلح هستند،” میگوید گاجانان کاتکار از UC San Diego. “برای اولین بار هوش مصنوعی این امکان را به ما داد تا بازیکنان دو تیم مخالف را بهوضوح شناسایی و پیگیری کنیم.”
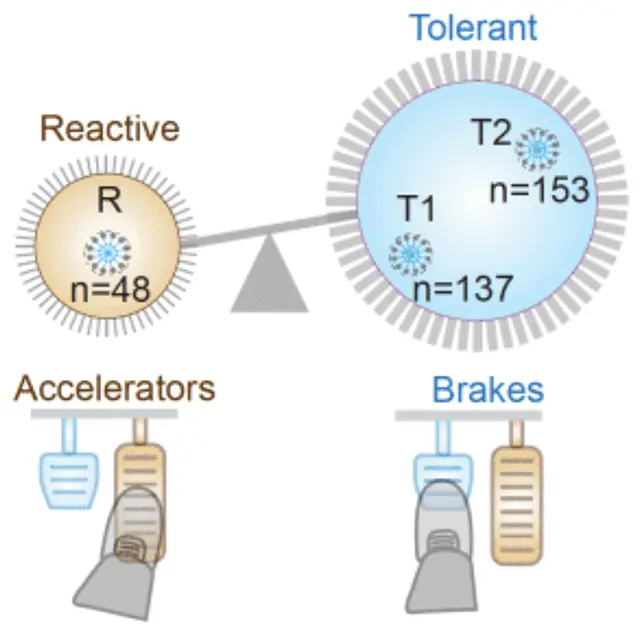
ماکروفاژهای روده میتوانند بین دو وضعیت تغییر کنند: یک وضعیت برای حمله به عفونت (التهابزا) و وضعیت دیگر برای تعمیر آسیب (غیرالتهابزا). بهخوبی ثابت شده است که حفظ تعادل بین این دو وضعیت برای داشتن رودهای سالم ضروری است.
تیم تحقیقاتی یک امضای ژنی شامل ۵۳ ژن تدوین کرد که وضعیت ماکروفاژها در IBD را تنظیم میکرد.
یک ژن که برای تقویت حالت ماکروفاژ غیرالتهابزا بهکار میرود، پروتئینی به نام girdin تولید میکند. معلوم شد که پروتئینهای girdin و NOD2 با هم همکاری میکنند تا ماکروفاژها نسبت به تهدیدها هوشیار بمانند، اما بیشفعال نباشند. در غیاب این دو پروتئین، ماکروفاژهای در حالت ترمیم کمکارآمدتر در پاکسازی اهداف میشوند، در حالی که ماکروفاژهای در حالت حمله بیشحدی التهابی میشوند.
“NOD2 بهعنوان سامانه نظارت بر عفونتهای بدن عمل میکند،” میگوید پردیپتا گُوش (Pradipta Ghosh) از UC San Diego. “هنگامی که به girdin پیوند میخورد، عوامل بیماریزا را شناسایی میکند و با خنثیسازی سریع آنها، تعادل ایمنی روده را حفظ مینماید.”
“بدون این همکاری، سامانه نظارت NOD2 فرو میریزد.”
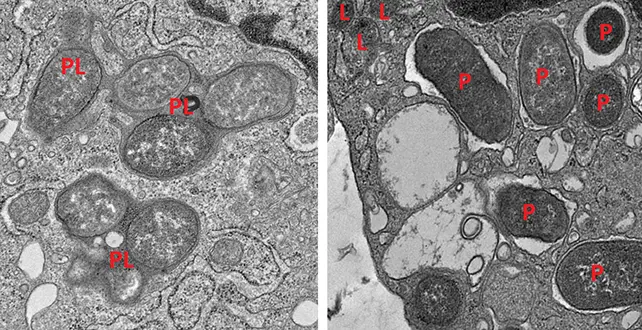
آزمایشهای تکمیلی بر روی موشها نتایج را تأیید کردند: موشهای فاقد girdin به التهاب روده دچار شدند و اغلب بهدلیل سپسیس، که ناشی از واکنش بیش از حد سیستم ایمنی است، کشته شدند.
این موضوع به ما درک بسیار بهتری از عدم تعادلی که در پیشبرد IBD مشارکت دارد و نقش خاص NOD2 در بیماری کرون میبخشد. کرون بهنظر میرسد که ناشی از چندین عامل همپوشانی باشد، اما این جهش بهنظر میرسد بخش عمدهای از تصویر کلی را تشکیل میدهد.
همانطور که همیشه در اینگونه پژوهشها مشاهده میشود، شناسایی ژنهای مسئول برخی بیماریها فرصتی برای توسعه درمانهای هدفمند فراهم میآورد؛ بهطوریکه شاید روزی داروهایی داشته باشیم که بتوانند جمعیت ماکروفاژهای روده را به همانگونه که NOD2 و girdin تعادل میدهند، حفظ کنند.
«این بینشها نور جدیدی بر مسیرهای مولکولی پایهدار بههمزیستی روده و پیشرفت IBD میتابانند و راههای درمانی بالقوهای برای بازگرداندن تعادل در زیرجمعیتهای ماکروفاژ ارائه میدهند»، پژوهشگران در مقاله منتشر شده خود نتیجهگیری میکنند.
این پژوهش در Journal of Clinical Investigation منتشر شده است.
